Natrijum sulfid
 | |
 | |
| Nazivi | |
|---|---|
| Drugi nazivi Dinatrijum sulfid | |
| Identifikacija | |
| |
3D model (Jmol) |
|
| ECHA InfoCard | 100.013.829 |
| EC broj | 215-211-5 |
| |
| RTECS | WE1905000 |
| UN broj | 1385 (anhidrat) 1849 (hidrat) |
SMILES
| |
| Svojstva | |
| Na2S | |
| Molarna masa | 78,0452 g/mol (anhidrat) 240,18 g/mol (nonahidrat) |
| Agregatno stanje | bezbojna, higroskopna čvrsta materija |
| Miris | pokvarena jaja |
| Gustina | 1,856 g/cm3 (anhidrat) 1,58 g/cm3 (pentahidrat) 1,43 g/cm3 (nonohidrat) |
| Tačka topljenja | 1176 °C (anhidrat) 100 °C (pentahidrat) 50 °C (nonhidrat) |
Rastvorljivost u vodi | 12,4 g/100 mL (0°C) 18,6 g/100 mL (20°C) 39 g/100 mL (50°C) |
| Rastvorljivost | nerastvoran u etru u maloj meri rastvoran u alkoholu |
| Struktura | |
| Kristalna rešetka/struktura | Antifluorit (kubna), cF12 |
| Kristalografska grupa | Fm3m, No. 225 |
| Geometrija molekula | Tetraedralna (Na+); kubna (S2–) |
| Opasnosti | |
| Bezbednost prilikom rukovanja | ICSC 1047 |
EU klasifikacija (DSD) | Korozivan (C) Opasan za životnu sredinu (N) |
| R-oznake | R31, R34, R50 |
| S-oznake | (S1/2), S26, S45, S61 |
| NFPA 704 |  1 3 1 |
Tačka spontanog paljenja | 480 °C (896 °F; 753 K) |
| Srodna jedinjenja | |
Drugi anjoni | Natrijum oksid Natrijum selenid Natrijum telurid |
Drugi katjoni | Litijum sulfid Kalijum sulfid |
Srodna jedinjenja | Natrijum hidrosulfid |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
 Y verifikuj (šta je Y verifikuj (šta je  Y Y Н ?) Н ?) | |
| Reference infokutije | |
Natrijum sulfid je hemijsko jedinjenje sa formulom Na2S, ili češće u hidratnom obliku, Na2S·9H2O. Oba oblika su bezbojne u vodi rastvorne soli koje formiraju jake alkaline rastvore. Kad su izloženi vlažnom vazduhu, Na2S i njegovi hidrati emituju vodonik sulfid, koji ima zadah pokvarenh jaja. Neki komercijalni uzorci su specificirani kao Na2S·xH2O, gde je težinski procenat Na2S specificiran.
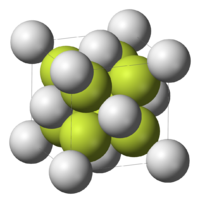
Struktura
Na2S poprima antifluoritnu strukturu,[3][4] što znači da Na+ centeri zauzimaju mesta fluorida u CaF2 poretku, a veći S2− zauzimaju mesta Ca2+. U rastvoru se soli disociraju. Dianjon S2− nije prisutan u značajnim količinama u vodi. Sulfid je suviše jaka baza da koegzistira sa vodom.
Produkcija
Industrijski Na2S se proizvodi redukcijom Na2SO4 ugljenikom, u obliku uglja:[5]
- Na2SO4 + 4 C → Na2S + 4 CO
U laboratoriji, anhidratna so se može pripremiti redukcijom sumpora natrijumom u anhidratnom amonijaku. Alternativno, sumpor se može redukovati natrijumom u suvom THF-u sa katalitičkom količinom naftalena:[6]
- 2 Na + S → Na2S
Reakcije
Proces rastvaranja se može opisati sledećom reakcijom:
- Na2S + H2O → 2Na+ + HS− + OH−
Natrijum sulfid se može oksidovati zagrevanjem do natrijum karbonata i sumpor dioksida:
- 2 Na2S + 3 O2 + 2 CO2 → 2 Na2CO3 + 2 SO2
Nakon tretmana sumporom, se formiraju polisulfidi:
- 2Na2S + S8 → 2 Na2S5
Reference
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003. уреди
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Zintl, E; Harder, A; Dauth, B. (1934). „Gitterstruktur der oxyde, sulfide, selenide und telluride des lithiums, natriums und kaliums”. Zeitschrift für Elektrochemie und Angewandte Physikalische Chemie. 40: 588—93.
- ^ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ So, J.-H; Boudjouk, P; Hong, Harry H.; Weber, William P. (1992). „Hexamethyldisilathiane”. Inorganic Syntheses. Inorganic Syntheses. 29: 30. doi:10.1002/9780470132609.ch11. ISBN 978-0-470-13260-9.
Spoljašnje veze
- п
- р
- у
- NaAlO2
- NaBH3(CN)
- NaBH4
- Na2B4O7 10 H2O
- NaBr
- NaBrO3
- NaCH3COO
- NaCFH2COO
- NaHCOO
- NaCN
- NaC6H5CO2
- NaC6H4(OH)CO2
- NaC18H35O2
- NaCl
- NaClO
- NaClO2
- NaClO3
- NaClO4
- NaF
- NaH
- NaHCO3
- NaH2PO4
- Na2HPO4
- Na3PO4
- NaHSO3
- NaHSO4
- NaI
- NaIO3
- NaIO4
- NaMnO4
- NaNH2
- NaNO2
- NaNO3
- NaN3
- NaOH
- NaO2
- NaPO2H2
- NaReO4
- NaSCN
- NaSH
- NaTcO4
- NaVO3
- Na2CO3
- 2 Na2CO3 3 H2O2
- Na2C2O4
- Na2CrO4
- Na2Cr2O7
- Na2MnO4
- Na2MoO4
- Na2O
- Na2O2
- Na2O(UO3)2
- Na2S
- Na2SO3
- Na2SO4
- Na2S2O3
- Na2S2O4
- Na2S2O5
- Na2S2O6
- Na2S2O7
- Na2S2O8
- Na2Se
- Na2SeO3
- Na2SeO4
- Na2SiO3
- Na2Te
- Na2TeO3
- Na2Ti3O7
- Na2U2O7
- NaWO4
- Na2Zn(OH)4
- Na3N
- Na3P
- Na3VO4
- Na4Fe(CN)6
- Na5P3O10
- NaBiO3











